
科学研究
科研进展
干细胞院合作揭示控制灵长类衰老的节律开关
2022-03-15
昼夜节律机制调节哺乳动物的睡眠-觉醒周期、新陈代谢、免疫功能和繁殖等生理活动与外界24小时昼夜循环相协同,从而维持机体组织和细胞生理活动的动态平衡。节律紊乱通常被认为是机体加速衰老的重要诱因。然而,核心节律机制如何调控灵长类的衰老仍知之甚少。
2022年3月15日,干细胞与再生医学研究院刘光慧研究组、中山大学项鹏研究组与干细胞与再生医学研究院曲静研究组合作在Nucleic Acids Research杂志在线发表题为“BMAL1 moonlighting as a gatekeeper for LINE1 repression and cellular senescence in primates”的研究论文。该研究通过CRISPR/Cas9介导的基因编辑技术产生了BMAL1缺失的人干细胞和非人灵长类研究模型,揭示了核心节律蛋白BMAL1具有维持基因组稳定性、抑制转座子LINE1活化,并拮抗灵长类组织和细胞衰老的新型功能。
BMAL1是生物钟最核心的组分之一,它作为转录因子在维持细胞分子生物钟和个体节律方面发挥着重要作用。迄今为止,BMAL1蛋白在灵长类细胞稳态及衰老中的调控作用尚不明确。在该研究中,研究人员发现人和猴细胞衰老过程中BMAL1逐渐从细胞核中排空,提示BMAL1可能与细胞衰老的基因表达调控相关。为研究BMAL1对灵长类细胞衰老的调控功能,研究人员结合CRISPR/Cas9介导的基因编辑技术和干细胞定向分化技术获得了BMAL1敲除的人间充质干细胞,进而发现BMAL1蛋白的缺失引起人间充质干细胞的加速衰老。虽然BMAL1依赖于其转录活性参与节律调节,但野生型BMAL1及其转录活性丧失的突变体均可抑制BMAL1缺失所致人间充质干细胞加速衰老,说明BMAL1对衰老的调控不依赖于经典的转录功能。深入的机制研究发现,BMAL1与核纤层及异染色质蛋白结合,有助于维持异染色质的结构稳定性,进而抑制“跳跃基因”LINE1的活化。BMAL1的缺乏导致LINE1等“核酸垃圾”在胞浆内表达和聚集,进而诱导下游cGAS-STING天然免疫通路的激活,加速干细胞衰老。反转录酶抑制剂拉米夫定(Lamivudine)处理可有效抑制BMAL1缺失引起的细胞加速衰老。同时,研究人员发现BMAL1缺失的猴间充质干细胞以及组织中也存在LINE1及cGAS-STING通路的激活,说明BMAL1抑制“垃圾核酸”积聚、稳定天然免疫通路的新功能在人和非人灵长类中保守。
该项研究首次揭示了核心节律蛋白抑制LINE1-cGAS-STING通路进而调控灵长类衰老的新功能及新机制。这一研究成果拓展了人们对核心节律蛋白生物学功能的认识,建立了昼夜节律和衰老调控的科学联系,为延缓灵长类衰老提供了新的分子靶标,同时为防治衰老相关疾病开拓了新的思路。
该研究工作由中国科学院动物研究所、中山大学中山医学院、中国科学院北京基因组研究所、首都医科大学宣武医院、北京干细胞与再生医学研究院、北京协和医院、香港中文大学医学院等多家机构合作完成。中国科学院动物研究所博士研究生梁楚倩、中山大学柯琼副教授、中国科学院动物研究所博士研究生刘尊鹏、中国科学院北京基因组研究所任捷研究员和张维绮研究员为并列第一作者。中国科学院动物研究所刘光慧研究员、中山大学项鹏教授和中国科学院动物研究所曲静研究员为文章的共同通讯作者。该研究得到了王华婷教授、孙昊教授和龙笑教授的支持,并获得科技部、国家自然科学基金委、中国科学院及北京市等项目的资助。
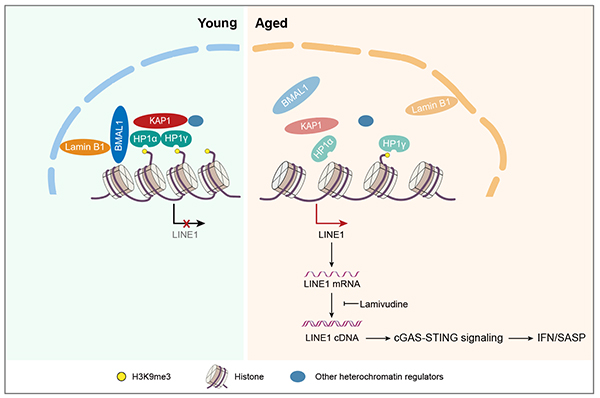
图:衰老伴随的BMAL1核内利用度降低导致LINE1激活,进而加速细胞衰老。
原文链接:https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkac146/6548307?login=true
附件:
