
科学研究
科研进展
干细胞院合作揭示控制灵长类衰老的节律开关
2022年3月15日,干细胞与再生医学研究院刘光慧研究组、中山大学项鹏研究组与干细胞与再生医学研究院曲静研究组合作在Nucleic Acids Research杂志在线发表题为“BMAL1 moonlighting as a gatekeeper for LINE1 repression and cellular senescence in primates”的研究论文。该研究通过CRISPR/Cas9介导的基因编辑技术产生了BMAL1缺失的人干细胞和非人灵长类研究模型,揭示了核心节律蛋白BMAL1具有维持基因组稳定性、抑制转座子LINE1活化,并拮抗灵长类组织和细胞衰老的新型功能。
2022-03-15
昼夜节律机制调节哺乳动物的睡眠-觉醒周期、新陈代谢、免疫功能和繁殖等生理活动与外界24小时昼夜循环相协同,从而维持机体组织和细胞生理活动的动态平衡。节律紊乱通常被认为是机体加速衰老的重要诱因。然而,核心节律机制如何调控灵长类的衰老仍知之甚少。
2022年3月15日,干细胞与再生医学研究院刘光慧研究组、中山大学项鹏研究组与干细胞与再生医学研究院曲静研究组合作在Nucleic Acids Research杂志在线发表题为“BMAL1 moonlighting as a gatekeeper for LINE1 repression and cellular senescence in primates”的研究论文。该研究通过CRISPR/Cas9介导的基因编辑技术产生了BMAL1缺失的人干细胞和非人灵长类研究模型,揭示了核心节律蛋白BMAL1具有维持基因组稳定性、抑制转座子LINE1活化,并拮抗灵长类组织和细胞衰老的新型功能。
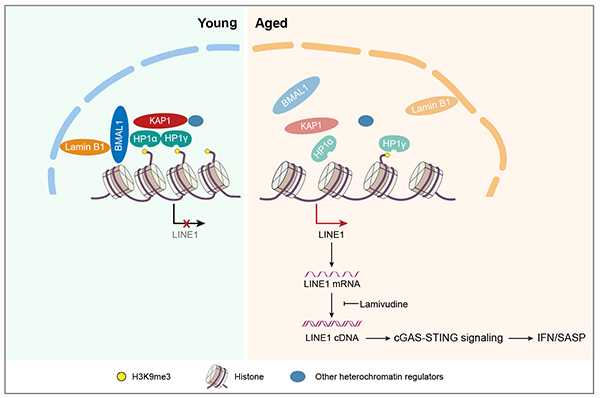
BMAL1是生物钟最核心的组分之一,它作为转录因子在维持细胞分子生物钟和个体节律方面发挥着重要作用。迄今为止,BMAL1蛋白在灵长类细胞稳态及衰老中的调控作用尚不明确。在该研究中,研究人员发现人和猴细胞衰老过程中BMAL1逐渐从细胞核中排空,提示BMAL1可能与细胞衰老的基因表达调控相关。为研究BMAL1对灵长类细胞衰老的调控功能,研究人员结合CRISPR/Cas9介导的基因编辑技术和干细胞定向分化技术获得了BMAL1敲除的人间充质干细胞,进而发现BMAL1蛋白的缺失引起人间充质干细胞的加速衰老。虽然BMAL1依赖于其转录活性参与节律调节,但野生型BMAL1及其转录活性丧失的突变体均可抑制BMAL1缺失所致人间充质干细胞加速衰老,说明BMAL1对衰老的调控不依赖于经典的转录功能。深入的机制研究发现,BMAL1与核纤层及异染色质蛋白结合,有助于维持异染色质的结构稳定性,进而抑制“跳跃基因”LINE1的活化。BMAL1的缺乏导致LINE1等“核酸垃圾”在胞浆内表达和聚集,进而诱导下游cGAS-STING天然免疫通路的激活,加速干细胞衰老。反转录酶抑制剂拉米夫定(Lamivudine)处理可有效抑制BMAL1缺失引起的细胞加速衰老。同时,研究人员发现BMAL1缺失的猴间充质干细胞以及组织中也存在LINE1及cGAS-STING通路的激活,说明BMAL1抑制“垃圾核酸”积聚、稳定天然免疫通路的新功能在人和非人灵长类中保守。
该项研究首次揭示了核心节律蛋白抑制LINE1-cGAS-STING通路进而调控灵长类衰老的新功能及新机制。这一研究成果拓展了人们对核心节律蛋白生物学功能的认识,建立了昼夜节律和衰老调控的科学联系,为延缓灵长类衰老提供了新的分子靶标,同时为防治衰老相关疾病开拓了新的思路。
该研究工作由中国科学院动物研究所、中山大学中山医学院、中国科学院北京基因组研究所、首都医科大学宣武医院、北京干细胞与再生医学研究院、北京协和医院、香港中文大学医学院等多家机构合作完成。中国科学院动物研究所博士研究生梁楚倩、中山大学柯琼副教授、中国科学院动物研究所博士研究生刘尊鹏、中国科学院北京基因组研究所任捷研究员和张维绮研究员为并列第一作者。中国科学院动物研究所刘光慧研究员、中山大学项鹏教授和中国科学院动物研究所曲静研究员为文章的共同通讯作者。该研究得到了王华婷教授、孙昊教授和龙笑教授的支持,并获得科技部、国家自然科学基金委、中国科学院及北京市等项目的资助。
图:衰老伴随的BMAL1核内利用度降低导致LINE1激活,进而加速细胞衰老。
原文链接:https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkac146/6548307?login=true
干细胞院合作解析人类胚胎不同脑区小胶质细胞发育
2022年3月3日,干细胞与再生医学研究院焦建伟研究组、北京大学杜鹏研究组、干细胞与再生医学研究院王雁玲研究组、北京大学靳蕾研究组合作在Cell Stem Cell 杂志在线发表了题为Decoding the Temporal and Regional Specification of Microglia in the Developing Human Brain的研究论文。该研究首次解析了人脑发育中不同区域的小胶质细胞单细胞转录组,精准揭示了发育中人脑小胶质细胞区域特化和状态转换的时空动力学特征,并通过比较小鼠和人类皮层小胶质细胞转录组差异,评估了这两个物种之间状态转换的保守性和分子差异性。
2022-03-03
作为中枢神经系统(Central Nervous System,CNS)的固有免疫细胞,小胶质细胞(Microglia)在健康CNS中发挥着重要的免疫、监测和保护作用。有证据表明,小胶质细胞来源于卵黄囊组织中的红髓系前体细胞,它们迁移、定植、分化,并在大脑中成熟,最终达到稳定状态,维持中枢神经系统环境的免疫平衡。与成年成熟的小胶质细胞相比,胚胎期小胶质细胞表现出很大的异质性,并参与各种生理活动的调节。中枢神经系统由脑和脊髓组成,脑主要区域包含大脑皮层、间脑、中脑和小脑。但是,起源于卵黄囊组织中红髓系前体细胞的小胶质细胞在四个脑区的发育路径和不同状态转换,以及它们的相关功能特征尚不清楚。
近年来,快速发展的单细胞组学技术,为理解细胞命运决定和细胞异质性提供了强有力的工具。之前对小鼠的单细胞测序研究结果显示,小胶质细胞具有高度异质性。然而,人类和小鼠之间的物种差异极大地限制了我们对人类小胶质细胞分化和发育功能的理解,尤其是在早期胚胎发育期间。此外,迄今为止,人类单细胞测序研究仅研究了小胶质细胞的早期起源,从卵黄囊到大脑进入前,或整个CNS中小胶质细胞的发育,对于人脑早期发育过程中小胶质细胞的区域特化命运决定和状态转换并不清楚。
2022年3月3日,干细胞与再生医学研究院焦建伟研究组、北京大学杜鹏研究组、干细胞与再生医学研究院王雁玲研究组、北京大学靳蕾研究组合作在Cell Stem Cell 杂志在线发表了题为Decoding the Temporal and Regional Specification of Microglia in the Developing Human Brain的研究论文。该研究首次解析了人脑发育中不同区域的小胶质细胞单细胞转录组,精准揭示了发育中人脑小胶质细胞区域特化和状态转换的时空动力学特征,并通过比较小鼠和人类皮层小胶质细胞转录组差异,评估了这两个物种之间状态转换的保守性和分子差异性。
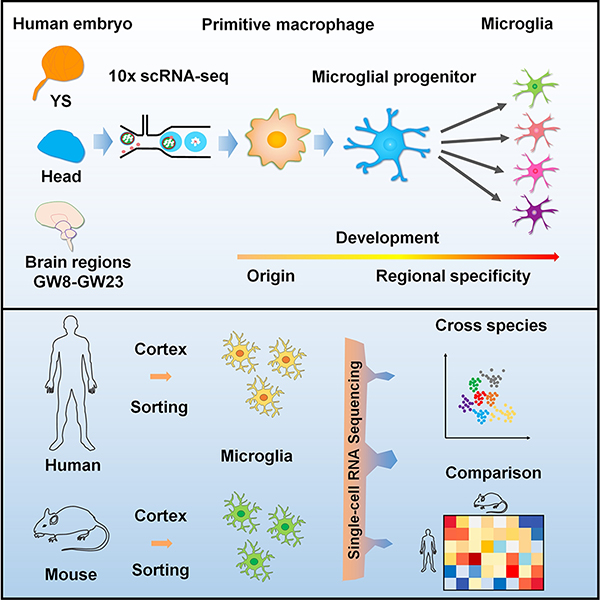
利用10x Genomics单细胞测序技术,作者绘制了来自人类胚胎,包括Carnegie Stage (CS)12卵黄囊和头部组织以及脑的不同解剖位置,包括大脑、间脑、中脑、小脑在多个孕周(gastrulation week,GW)(GW8、GW10、GW12、GW16和GW23)的单细胞转录组图谱。在进行质量控制和生物信息学聚类分析后,作者选择CD45+CD33+髓系细胞(共12565个细胞)进行分析。基于已知标记基因,该项研究识别了20个小胶质细胞亚群,并揭示上述群体的发育动力学特征。同时,根据基因表达特征将这些亚群分成了起源、增殖、免疫应答和神经元基因富集相关四大类。为了可视化和重塑来自CS12同一群原始髓系前体细胞的神经元基因富集小胶质细胞和免疫相关小胶质细胞的细胞命运决定轨迹,作者使用Monocle2和URD进行伪时间分析。有趣的是,两种分析方法均显示出类似的结果:源自CS12卵黄囊和头部的小胶质祖细胞首先启动细胞增殖,在不同的细胞周期阶段成为增殖的小胶质细胞,然后这些增殖的小胶质细胞向两种不同的细胞命运过渡:免疫或神经元基因富集特征。对于免疫相关的发育分枝,小胶质细胞通过一个共同的中间阶段,最终在GW23达到区域特化。然而,具有不同区域特征的神经元基因富集小胶质细胞可以直接从循环小胶质细胞而来。这是首次揭示了人胚胎脑神经元基因富集的小胶质细胞命运分枝。在这项研究中,作者鉴定出7群富含神经元基因的小胶质细胞,发现均瞬时出现在包括大脑、间脑、中脑和小脑的四个不同区域,且早在GW8(CNS区域形成的时期)时就在早期脑发育的不同阶段出现。稳态指小胶质细胞的一种静息状态,脱离静息状态会导致多种免疫应答反应的激活。在此,作者分析了胎儿小胶质细胞的区域特异性和状态转换之间的潜在联系。此研究首次提出免疫相关小胶质细胞的区域特化会伴随小胶质细胞静息状态的退出。接下来,作者进一步探究了GW23区域特化胎儿小胶质细胞的不同免疫激活状态。上述研究结果概述了具有区域特异性的免疫相关小胶质细胞的胎儿激活的独特特征,这与之前报道的所有成人成熟小胶质细胞明显不同。进一步,作者比较了人类和小鼠的小胶质细胞静息状态转变发现胎儿小胶质细胞的动态静息/活动状态转换在人类和小鼠中是保守的。将人鼠小胶质细胞拟合后,作者发现大多数其他细胞类型可以合并在一起,表明人类和小鼠的几种细胞类型和发育途径是保守的。此外,通过分析差异表达基因,发现人和小鼠小胶质细胞的分子特征存在一些差异。
综上所述,这项研究揭示了人类胚胎小胶质细胞从卵黄囊到脑不同区域的整体发育路径、区域异质性、胎儿小胶质细胞状态转变的独特特征,以及早期大脑发育期间状态转变和区域特异性之间的密切联系,这些发现将为研究小胶质细胞正常功能及相关疾病机理研究提供重要的理论基础。
焦建伟、杜鹏、王雁玲和靳蕾为该论文的共同通讯作者。博士后李妍昕、博士后李忠秋、博士研究生杨敏、博士后王飞扬、张玥红主任医师、李蓉主任医师为该论文的共同第一作者。滕兆乾研究团队参与了项目协作。该研究获得了国家科技部、国家自然科学基金委、中国科学院先导等项目的资助。
文章链接:https://doi.org/10.1016/j.stem.2022.02.004
干细胞院合作发现促进多组织再生、延缓衰老的小分子代谢物
2022年2月1日,干细胞与再生医学研究院刘光慧研究组、曲静研究组和中国科学院北京基因组研究所张维绮研究组合作,于Cell Discovery杂志在线发表题为“Cross-species metabolomic analysis identifies uridine as a potent regeneration promoting factor”的研究论文。该研究深度解析了跨物种、跨年龄、跨组织的代谢分子特征,解码了与较高再生能力密切相关的代谢调节通路,鉴定了一系列能改够延缓人类干细胞衰老、促进多组织再生的关键通路和小分子代谢物,为衰老的科学评估、衰老相关疾病的防治以及再生医学的发展提供了潜在的分子标记物和干预策略。
2022-02-02
再生是机体修复受损、病变或衰老组织的重要过程。从低等动物到人类,不同物种具有不同程度的再生能力,并且这种能力随着物种的不断进化而逐步降低。例如,低等动物中的蝾螈能够实现断肢的完全再生,而包括人类在内的大多数哺乳动物仅具备有限的再生和损伤修复能力。在哺乳动物中,鹿角是唯一能够完全再生的器官。尽管高度进化的物种能在组织损伤时启动相应的再生修复程序,但这种再生修复的能力会随着年龄的增长而逐渐降低。众所周知,干细胞在组织再生和修复的过程中发挥着关键作用。例如,蝾螈可以通过形成芽基组织(一群去分化的具有干性的细胞)来完成肢体的再生。同样地,在每年的鹿角再生过程中,位于鹿角骨膜的鹿茸干细胞可以分化产生包含血管、软骨、骨、真皮和神经在内的完整鹿角器官。人类成体干细胞,如间充质干细胞,在多种组织和器官的再生修复过程中均起到关键作用,但是这些干细胞的数量和再生能力同样会随着机体年龄的增加而降低。
虽然人们已经发现机体再生能力随进化和衰老而逐步丧失的规律,但其中的分子机制尚不明确。内源性小分子代谢物在不同物种间相对保守;然而,迄今为止,人们对能够调节衰老和再生的小分子代谢物还知之甚少。通过向自然界存在的低等动物的再生过程学习、以及向具有较强再生能力的年轻组织和干细胞学习,理论上有望发现跨物种保守的、调节再生和衰老的关键代谢小分子,从而将为解码再生的代谢调控机制,发现促进再生、延缓衰老的关键代谢物提供新的线索和思路。
2022年2月1日,干细胞与再生医学研究院刘光慧研究组、曲静研究组和中国科学院北京基因组研究所张维绮研究组合作,于Cell Discovery杂志在线发表题为“Cross-species metabolomic analysis identifies uridine as a potent regeneration promoting factor”的研究论文。该研究深度解析了跨物种、跨年龄、跨组织的代谢分子特征,解码了与较高再生能力密切相关的代谢调节通路,鉴定了一系列能改够延缓人类干细胞衰老、促进多组织再生的关键通路和小分子代谢物,为衰老的科学评估、衰老相关疾病的防治以及再生医学的发展提供了潜在的分子标记物和干预策略。
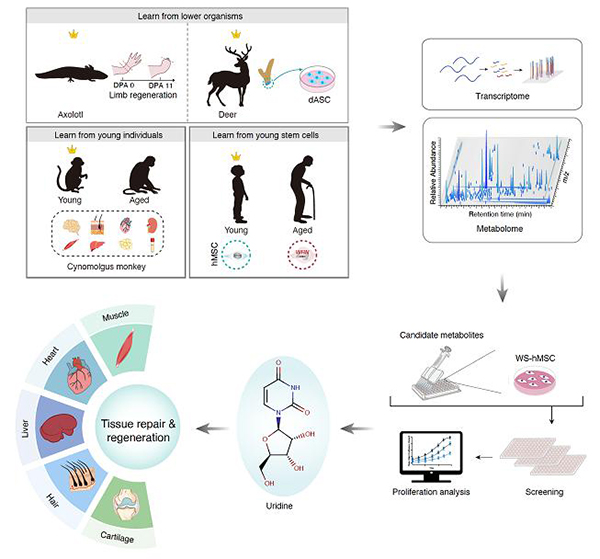
该研究通过跨物种、跨年龄、跨组织地绘制多种细胞类型的代谢图谱,其中包括:蝾螈断肢再生的芽基、鹿茸干细胞、年轻和年老食蟹猴的多种组织(脑、心脏、肝脏、肌肉、肾脏、脂肪、皮肤、血液)以及年轻和衰老的间充质干细胞,系统揭示了一些跨物种保守的、再生相关的代谢通路。例如,再生能力强的生物样本更倾向于富集多胺代谢、尿嘧啶代谢和脂肪酸代谢通路。进一步结合人类干细胞衰老的研究平台,研究人员对潜在的促再生代谢物进行了细致的筛选,发现小分子代谢物尿苷(Uridine)可以明显提升衰老人间充质干细胞的自我更新能力。进一步研究表明,尿苷处理可以在5种小鼠的组织损伤模型(肌肉损伤模型、肝纤维化模型、毛发再生模型、心肌梗塞模型和关节炎模型)中助力损伤或病变组织的再生修复。在肌肉损伤模型中,尿苷有效提升了肌肉的再生修复能力、缓解了肌肉损伤引起的炎症反应,同时增强了小鼠的肢体抓力和系统运动能力;在肝脏纤维化模型中,尿苷缓解了四氯化碳诱导的肝纤维化,有效改善了肝功能的多个生理指标;在毛发再生模型中,尿苷处理可以刺激毛囊提前进入生长期,从而促进毛发的生长;在心肌梗塞模型中,尿苷能有效缓解急性炎症、提升损伤心脏的收缩能力;在关节炎模型中,尿苷可以促进关节软骨再生、提升小鼠的关节运动能力。以上结果表明,单一代谢物尿苷能够促进哺乳动物多器官组织的再生修复过程。与年轻个体具有较强的再生能力一致,年轻人血液中具有比老年人更高的尿苷含量。接下来,研究人员进一步探究了尿苷处理是否可以增强老年个体的生理机能。结果发现,两个月的口服尿苷处理可以增强老年小鼠(22月龄)的生理机能,表现为肢体抓力和运动能力的显著提升。这些发现从多个层面证实了尿苷具有抑制人类干细胞衰老、促进多组织再生修复、提高老年个体生理机能的潜在活性。
该研究首次绘制了跨物种、跨年龄以及跨组织细胞的内源性代谢物的全景图谱,系统解析了强再生能力所伴随的分子代谢通路。更为重要的是,该研究发现尿苷是一种能延缓人类干细胞衰老、促进哺乳动物多组织再生修复的关键代谢物。这些发现为深入认识机体损伤或病理修复的机制奠定了理论基础,并为提升老年群体的健康、预防和治疗衰老相关疾病提供新的策略。
该研究的相关数据已同时上传至衰老多组学数据库Aging Atlas (AA, https://bigd.big.ac.cn/aging/index) 和再生多组学数据库Regeneration Roadmap (RR, https://ngdc.cncb.ac.cn/aging/index)。
该研究由中国科学院动物研究所、北京干细胞与再生医学研究院、首都医科大学宣武医院、中国科学院北京基因组研究所(国家生物信息中心)、北京医院、北京大学第三医院等机构合作完成。中国科学院动物研究所刘光慧研究员、曲静研究员、中国科学院北京基因组研究所张维绮研究员为论文的共同通讯作者。中国科学院动物研究所博士研究生刘尊鹏、首都医科大学宣武医院助理研究员李维和副研究员耿令令、北京医院孙亮教授、中国科学院北京基因组所博士研究生王俏然以及北京大学第三医院于洋教授为论文的共同第一作者。该研究得到了北京大学韩敬东教授、中国科学院北京基因组研究所任捷研究员、中国科学院动物研究所宋默识研究员和黄仕强研究员、首都医科大学宣武医院王思研究员和长春科技学院李春义教授的指导与支持,同时获得了国家科技部、国家自然科学基金委、中国科学院及北京市等项目的资助。
原文链接:https://www.nature.com/articles/s41421-021-00361-3
附图:通过跨物种和跨年龄的代谢组分析鉴定促进多组织修复、延缓衰老的关键代谢小分子。
赵勇研究组及合作者揭示组织定居记忆性T细胞可以介导器官移植物排斥
2022年1月26日,干细胞与再生医学研究院赵勇研究团队,中南大学湘雅二医院谢续标研究团队和北京朝阳医院泌尿外科王玮研究团队合作在Science Advances在线发表题为“Skin and heart allograft rejection solely by long-lived alloreactive TRM cells in skin of severe combined immunodeficient mice”的研究论文,首次揭示了定居在皮肤组织的记忆T细胞(TRM)可以单独介导同种异基因皮肤或心脏移植物的急性免疫排斥反应。
2022-01-26
临床器官移植是器官损伤终末期患者的有效治疗手段。受者免疫系统对心脏、肾脏等器官移植物的免疫排斥仍是临床面临的重要科学问题和限制移植物长期存活的重要障碍。然而,长期定居在非淋巴组织或其它器官中的识别同种异体抗原的记忆性T细胞(TRM)是否参与同种异基因移植物的排斥及其移植免疫排斥的特点等问题尚不清楚。2022年1月26日,干细胞与再生医学研究院赵勇研究团队,中南大学湘雅二医院谢续标研究团队和北京朝阳医院泌尿外科王玮研究团队合作在Science Advances在线发表题为“Skin and heart allograft rejection solely by long-lived alloreactive TRM cells in skin of severe combined immunodeficient mice”的研究论文(论文链接:https://www.science.org/doi/10.1126/sciadv.abk0270),首次揭示了定居在皮肤组织的记忆T细胞(TRM)可以单独介导同种异基因皮肤或心脏移植物的急性免疫排斥反应。
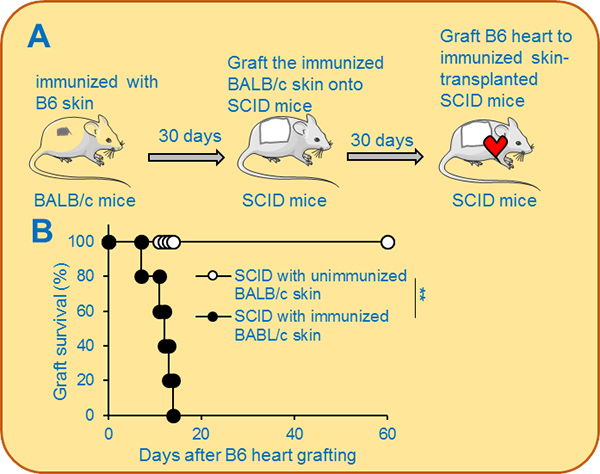
该研究使用T/B细胞缺失的免疫缺陷小鼠SCID或Rag2 KO小鼠,创新性地建立了一个单独研究致敏形成的组织定居记忆T细胞介导移植物排斥的小鼠实验模型。将同种异基因皮肤移植物用皮肤移植的方式致敏正常小鼠后30天或100天,将致敏的一块皮肤组织移植到MHC 匹配的免疫缺陷小鼠(SCID 或Rag2 敲除小鼠)。待小鼠恢复30天后,对其进行同种异基因皮肤或心脏移植实验观察。结果表明,预先移植致敏皮肤的免疫缺陷SCID或 Rag2 KO小鼠可以介导同种异基因或心脏移植物的急性排斥,而移植未致敏皮肤的SCID或 Rag2 KO小鼠则不能介导免疫排斥,使同种异基因皮肤或心脏移植物长期存活。证明皮肤组织定居的同种反应性TRM细胞单独就可以介导同种异基因皮肤物或心脏移植物的急性排斥。进一步实验研究发现,皮肤组织定居的同种反应性CD4+ 或者CD8+TRM细胞单独即可以急性排斥同种异基因移植物。该独特的移植小鼠模型的建立实现了在不受淋巴器官和组织的T/B淋巴细胞干扰或参与的情况下,研究其它组织如皮肤中长寿命同种异体反应TRM细胞在介导同种异体移植排斥反应中的作用及相关机制,对评价和鉴定靶向TRM细胞介导的同种异体移植排斥反应的新药具有重要意义价值。该研究提示,我们应重视受者组织TRM细胞在临床同种异体器官移植排斥反应中的重要作用。
中国科学院动物研究所赵勇研究员,中南大学湘雅二医院肾移植科谢续标教授和北京朝阳医院泌尿外科王玮教授为本文的共同通讯作者。中国科学院动物研究所移植生物学研究组博士生田倩川、张照奇,博士后杨帆和中南大学湘雅二医院谭亮博士为本文的共同第一作者。该研究得到基金委、科技部和中科院先导专项资助。
干细胞院近期取得生物3D/4D打印系列突破
生物3D/4D打印技术是器官体外再造的重要手段。近年来,打印技术已在多种组织器官构建中有所应用,但是工程手段的单一性无法满足器官复杂性的需求,尤其缺少多尺度管道连接以及微环境动态变化控制的策略;另外制造器官中的细胞空间运动规律不明、调控手段缺失。针对以上问题干细胞与再生医学研究院交叉学科团队(生物制造研究组:https://www.gulab.info)近期取得了以下系列成果。
2021-12-15
生物3D/4D打印技术是器官体外再造的重要手段。近年来,打印技术已在多种组织器官构建中有所应用,但是工程手段的单一性无法满足器官复杂性的需求,尤其缺少多尺度管道连接以及微环境动态变化控制的策略;另外制造器官中的细胞空间运动规律不明、调控手段缺失。针对以上问题干细胞与再生医学研究院交叉学科团队(生物制造研究组:https://www.gulab.info)近期取得了以下系列成果。
(1)一体化复杂管网组织打印
干细胞与再生医学研究院顾奇、中国科学院沈阳自动化研究所郑雄飞、中国科学院化学研究所王树研究团队协同攻关、耗时4年建立了复合打印系统实现多尺度管道的功能连接。联合团队开发了低粘度双分子互穿网络水凝胶,并调节高分子网络孔径促进人脐静脉内皮细胞(HUVECs)形成毛细血管的长度和分支点数以形成多分支毛细血管网;其次团队针对性设计双控温打印系统以实现低粘度复合水凝胶的精准成型;该系统已应用于肝组织的构建和体内移植(如图1)。相关研究工作作为内封面发表于先进生物材料杂志上Advanced Healthcare Materials,该论文第一作者为中国科学院动物研究所博士研究生刘鑫,并列第一作者包括中国科学院动物研究所特聘研究助理王新环博士、中国科学院沈阳自动化研究所张黎明、中国科学院分子细胞科学卓越创新中心孙露露。
(2)通过生物3D打印可控骨骼肌纤维的动态组装
仿生精准排列和可控动态控制是生物制造的难题,干细胞与再生医学研究院顾奇、黄仕强研究组以骨骼肌构建作为模型,报道了不同空间限制对细胞排列及分化影响,并提出了在这一过程中细胞和材料动态变化的假说,相关结果发表于国际生物制造杂志Biofabrication,该论文第一作者为中国科学院动物研究所博士研究生范婷婷。研究表明特定空间环境限制和响应性生物活性纤维材料促进了细胞形变、周围环境重塑,微观形变积累的机械能又进一步促进重塑过程,从而产生高取向大尺度肌肉组织结构(图2)。并研究揭示了生物制造组织三维构建过程中的动态变化,以及物理因素在细胞定向运动和功能化中的作用。
(3)基于纳米类囊体和热响应聚合物的仿生4D打印可呼吸式水凝胶致动器
中国科学院化学研究所王树、干细胞与再生医学研究院顾奇研究组联合报道了一种基于类囊体膜(纳米类囊体)和热响应聚合物的仿生4D打印可呼吸式水凝胶致动器。这种具有光热转换和催化特性的智能可呼吸式水凝胶致动器可以仿真模拟植物动态形变及产生O2等生命活动,同时具备水下可控运动的能力,比如通过打印的仿生机械手抓取物体,相关结果发表于国际杂志先进功能材料Advanced Functional Materials上。联合团队利用菠菜来源的纳米类囊体进行光热转换和H2O2的催化分解;借助热响应聚合物聚(N-异丙基丙烯酰胺)(PNIPA)产生变形力;并进一步利用4D打印双层聚(N-异丙基丙烯酰胺)/聚丙烯酰胺(PNIPA/PAA)的不对称结构放大机械运动(图3)。该研究工作为智能水凝胶设计提供了一种全新策略,为4D打印技术仿生能力提升开辟了新方向,并为自动化机器人和智能生物医学器件领域提供了极具前景的候选材料。
上述三个研究工作得到了中国科学院战略性先导科技专项“器官重建与制造”(XDA16020802, XDA16020803,XDA16020804),国家自然科学基金项目(21661132006,51875557),中国科学院青年团队项目(YSBR-012),中国科学院工程实验室项目(KFJ-PTXM-039),科技部重点研发计划(2020YFB1313100)等项目支持以及先导项目责任专家和监理专家的指导。
论文信息:
3D Liver Tissue Model with Branched Vascular Networks by Multimaterial Bioprinting
Xin Liu#, Xinhuan Wang#, Liming Zhang#, Lulu Sun#, Heran Wang, Hao Zhao, Zhengtao Zhang, Wenli Liu, Yiming Huang, Shen Ji, Jingjinqiu Zhang, Kai Li, Biaobiao Song, Chun Li, Hui Zhang, Song Li, Shu Wang,* Xiongfei Zheng,* and Qi Gu*
Advanced Healthcare Materials
DOI: 10.1002/adhm.202101405
原文链接:https://doi.org/10.1002/adhm.202101405
Controllable assembly of skeletal muscle-like bundles through 3D bioprinting
Tingting Fan, Shuo Wang, Zongmin Jiang, Shen Ji, Wenhua Cao, Wenli Liu, Yun Ji, Yujing Li,Ng Shyh-Chang*, and Qi Gu*
Biofabrication
DOI: 10.1088/1758-5090/ac3aca
原文链接:https://iopscience.iop.org/article/10.1088/1758-5090/ac3aca
Biomimetic 4D-Printed Breathing Hydrogel Actuators by Nanothylakoid and Thermoresponsive Polymer Networks
Hao Zhao, Yiming Huang, Fengting Lv, Libing Liu, Qi Gu,* and Shu Wang*
Advanced Functional Materials
DOI: 10.1002/adfm.202105544
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202105544
图1. 一体化打印具有分支血管网络的肝组织
图2. 骨骼肌组织体外构建
图3. 仿生4D打印可呼吸式水凝胶致动器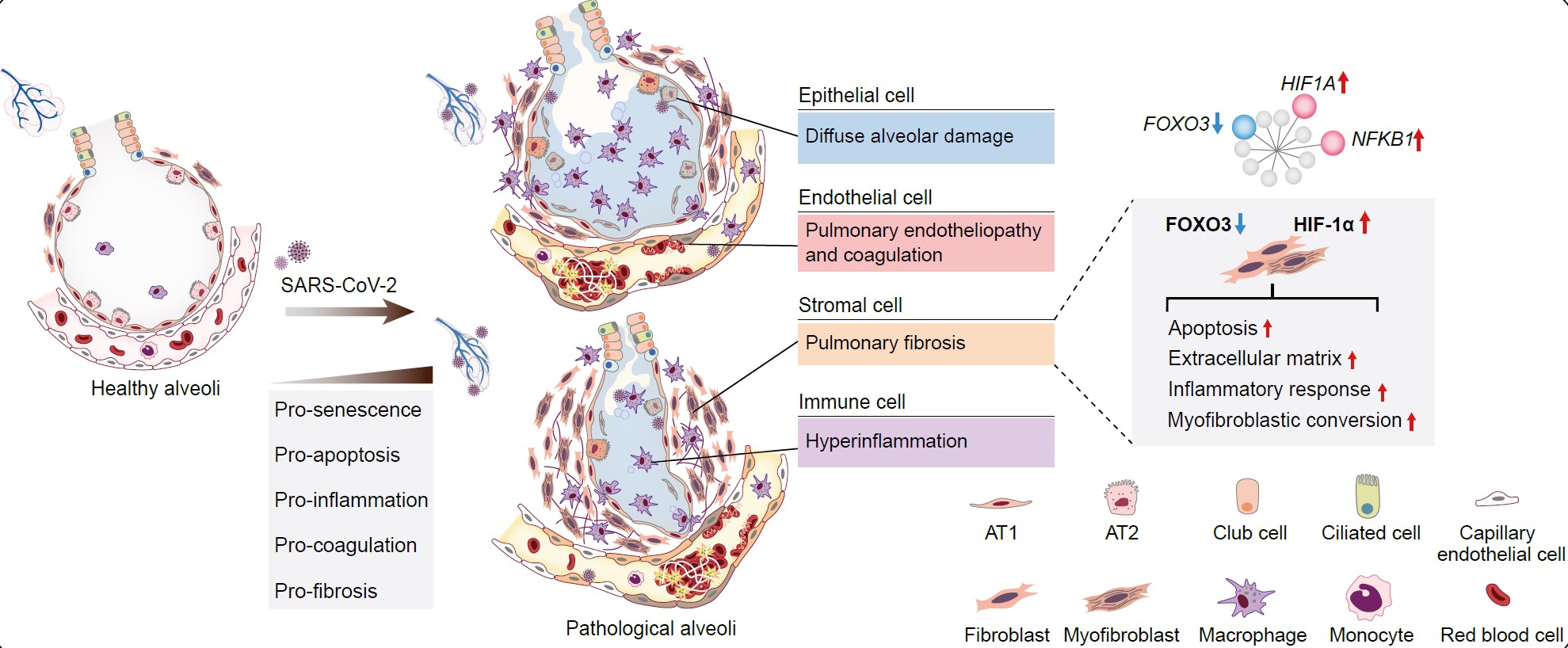
干细胞院合作研究揭示老年新冠肺炎患者肺损伤机制
12月8日,干细胞与再生医学研究院刘光慧研究组和曲静研究组、陆军军医大学(第三军医大学)第一附属医院(西南医院)卞修武研究组、中国科学院北京基因组研究所张维绮研究组合作,在Nature Cell Biology杂志在线发表题为“A single-cell transcriptomic landscape of the lungs of patients with COVID-19”的研究论文。研究结合病理学和高通量单细胞核转录组和蛋白质组等技术,深度解析了老年COVID-19患者肺组织的细胞和分子病理表型组特征,进一步认识了COVID-19肺损伤的关键细胞和分子机制,建立了肺衰老与COVID-19损伤的科学联系,为提高重症和危重症诊治水平提供了科学依据。
2021-12-08
新冠病毒(SARS-CoV-2)导致的新冠肺炎(COVID-19)已经引发全球大暴发,严重危害人类生命健康。据统计,住院死亡病例中70%以上为年龄超过65岁的老年人。与年轻群体相比,老年群体感染SARS-CoV-2后更易发展为重症和危重症,甚至死亡。肺是SARS-CoV-2感染和损伤的主要靶器官,严重肺损伤导致呼吸衰竭是COVID-19患者主要死因。COVID-19肺和其他脏器损伤机制研究已经不乏报道,但是基于老年患者尸检样本的肺组织病理与肺单细胞信息密切关联的多重损伤分子机制研究尚缺乏,对于老年患者更易出现重症和危重症的细胞和分子基础的认识远远不足。
12月8日,干细胞与再生医学研究院刘光慧研究组和曲静研究组、陆军军医大学(第三军医大学)第一附属医院(西南医院)卞修武研究组、中国科学院北京基因组研究所张维绮研究组合作,在Nature Cell Biology杂志在线发表题为“A single-cell transcriptomic landscape of the lungs of patients with COVID-19”的研究论文。研究结合病理学和高通量单细胞核转录组和蛋白质组等技术,深度解析了老年COVID-19患者肺组织的细胞和分子病理表型组特征,进一步认识了COVID-19肺损伤的关键细胞和分子机制,建立了肺衰老与COVID-19损伤的科学联系,为提高重症和危重症诊治水平提供了科学依据。
通过对COVID-19患者肺病变及其异质性的详细分析,研究人员发现肺两种上皮细胞脱落和凋亡的升高、炎症损伤与免疫反应的过度、不同血管内皮细胞的变化、凝血功能紊乱以及细胞表型转化与肺纤维化的加剧等事件是COVID-19肺病理的关键损伤过程和分子特征。进而,结合COVID-19患者肺组织的多维组学分析,研究人员首次发现肺组织的加速衰老是COVID-19的新型病理事件。具体而言,与年龄匹配的对照肺组织相比,老年COVID-19患者肺组织中的衰老标志物(p16、p21、p53)、衰老相关分泌表型因子(IL-6)、DNA氧化损伤标记物(8-OHdG)等均呈现上调表达,且核纤层蛋白(LAP2)和异染色质蛋白(HP1γ)表现为加速缺失。这些均提示SARS-CoV-2感染可诱发肺组织细胞的加速衰老。为进一步明确细胞类型特异的基因表达变化,研究人员利用高精度单核转录组测序技术,系统揭示了包括肺部上皮细胞、内皮细胞、基质细胞和免疫细胞4种主要细胞大类,28种不同细胞类型的病理相关基因表达特征。
对于肺上皮细胞而言,研究发现SARS-CoV-2感染导致上皮细胞凋亡和功能紊乱,主要表现为肺表面活性物质减少及粘液分泌增多,这可能与气体交换障碍及肺部低氧血症密切相关。此外,研究人员鉴定了一类Ⅱ型肺泡上皮细胞(AT2)向Ⅰ型肺泡上皮细胞(AT1)分化过程中的过渡态细胞类型,其具有损伤相关瞬时祖细胞(DATP)的特征。这类细胞亚群在COVID-19肺组织中大量聚集,可能是介导COVID-19肺上皮细胞缺失及损伤加剧的原因之一。进一步,研究人员通过对免疫细胞亚群的分析发现,肺泡及肺间质中促炎性巨噬细胞增加,这些细胞可能通过释放大量的促炎细胞因子加重弥漫性肺泡损伤。针对于血管内皮细胞的分析结果显示,SARS-CoV-2感染可能导致内皮损伤及凝血程序的启动。此外,研究人员还发现COVID-19肺组织中富集了一群介于肺毛细血管内皮和肺泡气体交换毛细血管内皮之间的毛细血管中间态细胞,这些细胞高表达血管内皮炎症和损伤相关基因,可能介导了内皮细胞分化特征的紊乱及COVID-19肺的内皮病变。此外,结合人肺成纤维细胞的研究模型,研究人员发现长寿基因FOXO3的表达沉默可能是成纤维细胞向肌成纤维细胞(介导肺纤维化的主要细胞类型)转变的关键驱动因素。这些发现为COVID-19肺损伤的发生发展提供了新型生物标志物和潜在干预靶标。
该研究报道了COVID-19患者肺组织的多维组学全景图谱,系统解析了COVID-19患者肺组织中多种细胞类型的疾病变化规律,加深了人们对COVID-19患者肺组织多种结构病变和功能减损的认识。更为重要的是,研究首次鉴定了COVID-19患者肺的加速衰老表型。考虑到衰老细胞累积对器官退行的驱动作用,该研究为SARS-CoV-2感染导致的老年人致死率增加及预后的多种后遗症提供了可能的解释。该研究为阐明COVID-19发病机制以及老年群体中新冠肺炎高重症率的原因提供了重要线索,并为发展新冠肺炎及老年群体愈后后遗症的干预策略提供了新思路。
相关数据已上传至衰老多组学数据库Aging Atlas (https://bigd.big.ac.cn/aging/index)。
该项目获得科技部、国家自然科学基金委、中科院和北京市等的资助。
论文链接:https://www.nature.com/articles/s41556-021-00796-6.pdf
示意图显示,上皮细胞衰老、脱落、凋亡升高、过度炎症反应、凝血和纤维化加剧是COVID-19肺的主要病理表型特征,也是全身系统性免疫损伤的“发源地”和“主战场”。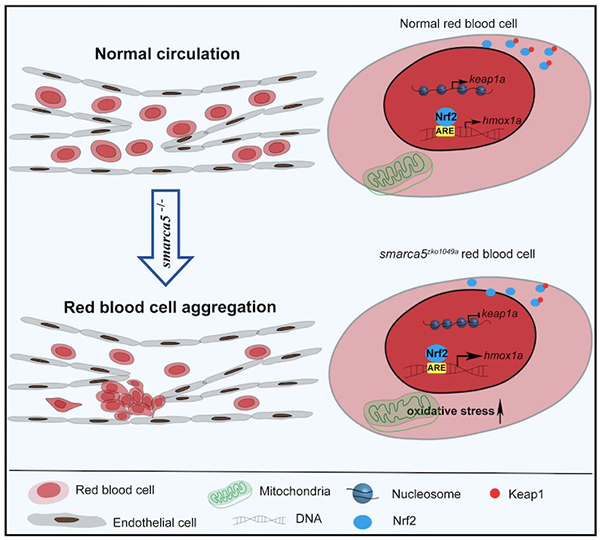
刘峰团队建立新型静脉血栓疾病模型
2021年10月26日,干细胞与再生医学研究院刘峰研究员团队在eLife杂志发表题为The chromatin-remodeling enzyme Smarca5 regulates erythrocyte aggregation via Keap1-Nrf2 signaling的论文。该工作发现:斑马鱼smarca5突变体红细胞发生异常聚集并沉积在尾部静脉。深入机制探索发现,Smarca5通过调控Keap1-Nrf2信号通路调节红细胞聚集。该红细胞聚集模型能部分模拟静脉血栓,为其作为血栓疾病模型进行发病机制探索和药物筛选奠定了基础。
2021-10-26
成熟的红细胞富含血红蛋白,具有携带氧气的功能,对维持机体的稳态至关重要1。红细胞缺陷会导致多种疾病的发生,包括血红蛋白异常性贫血、红细胞溶解性贫血以及血栓等2-4。其中,血栓的发生严重危害了人类的健康5。目前,结扎下腔静脉模型、自由基血栓形成模型和基因敲除模型等已被广泛应用于小鼠静脉血栓研究6-7。这些模型主要通过改变血流、损伤内皮以及调节凝集因子引发血栓形成。此外,苯肼处理可以通过损伤红细胞,导致其磷脂酰丝氨酸外翻以及自由基产生,进而引发血栓发生8。通过动物疾病模型研究血栓的发生,为探究其机制和寻找新的治疗手段提供了帮助。然而,血栓形成的动态过程以及红细胞参与的血栓形成机制仍有待探索。
2021年10月26日,干细胞与再生医学研究院刘峰研究员团队在eLife杂志发表题为The chromatin-remodeling enzyme Smarca5 regulates erythrocyte aggregation via Keap1-Nrf2 signaling的论文。该工作发现:斑马鱼smarca5突变体红细胞发生异常聚集并沉积在尾部静脉。深入机制探索发现,Smarca5通过调控Keap1-Nrf2信号通路调节红细胞聚集。该红细胞聚集模型能部分模拟静脉血栓,为其作为血栓疾病模型进行发病机制探索和药物筛选奠定了基础。
研究人员首先从smarca5突变体红细胞异常聚集的表型出发,进行血栓疾病模型的表型确认和机制研究。在smarca5突变体发育至受精后第2天,血细胞发生异常聚集并沉积在尾部静脉。通过荧光显微镜观察gata1:dsRed标记的红细胞在突变体中的聚集表型,研究人员发现,红细胞在突变体尾部静脉血管(kdrl:GFP)内发生聚集。随后,研究人员用血栓治疗药物Argatroban处理smarca5突变体,结果显示Argatroban处理可以部分缓解血块的产生。因此,smarca5突变体可以部分模拟血栓疾病。
染色质重塑因子Smarca5可以调节核小体间距,进而影响基因的转录9。为了探究smarca5缺失对红细胞转录组和染色质可接近性的影响,研究人员采用RNA-seq和ATAC-seq对smarca5突变体和对照组胚胎红细胞进行分析。基因组变异分析显示,smarca5突变后,红细胞中转录下降的基因主要与“Gata1下游靶点”, “红细胞携氧”等通路相关;而上调的基因主要与“应激反应”,“衰老”和“细胞氧化”等通路相关。在突变体组中染色质开放性和转录水平同时上调和下调的基因中,keap1a启动子区的染色质开放性以及转录表达在smarca5缺失后出现下降。Keap1-Nrf2系统是一种进化保守的氧化应激防御机制10-11。在细胞质中,Keap1可以与Nrf2结合,阻止Nrf2的入核以及下游靶基因的激活。在smarca5突变的红细胞中,研究人员发现Nrf2的靶基因被过度激活,其中包括hmox1a。Hmox1可以催化血红素降解为胆绿素、一氧化碳和Fe2+,因此hmox1的过度激活可引起细胞的氧化损伤12。为了进一步探究Keap1-Nrf2信号通路是否参与红细胞聚集的表型,研究人员在smarca5突变体胚胎中进行keap1a过表达或hmox1a敲降实验。结果显示,过表达keap1a或敲降hmox1a可部分减少红细胞的聚集。以上结果说明,smarca5部分通过Keap1-Nrf2信号通路调节红细胞异常聚集的表型。
综上所述,该研究首次发现了smarca5突变体红细胞异常聚集的表型,并初步解析了smarca5调控红细胞聚集的机制,与此同时,研究人员建立了一种新的静脉血栓疾病模型,为其作为血栓疾病模型并用于药物筛选等临床转化研究奠定基础。
干细胞与再生医学研究院刘峰研究员为论文通讯作者,生物岛实验室博士后丁岩岩、清华大学博士研究生李雨哲与中国科学院动物研究所硕士研究生赵梓倩为论文共同第一作者,清华大学张强锋教授参与此项工作。该研究得到了国家重点研发计划、国家自然科学基金以及中国科学院的资助。
文章链接:https://elifesciences.org/articles/72557
图示:smarca5突变体红细胞发生异常聚集
图示:Smarca5通过调控Keap1-Nrf2信号通路调节红细胞聚集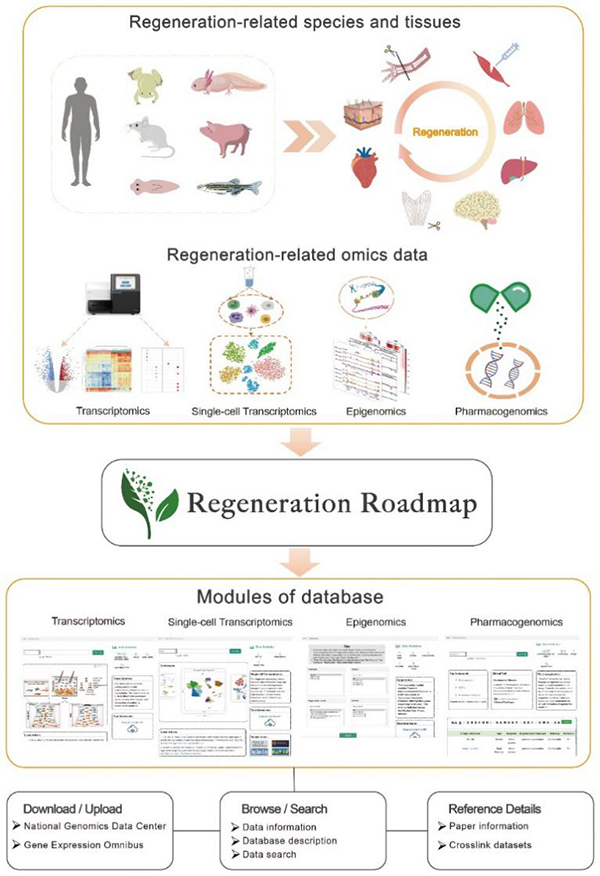
干细胞院合作创建再生生物学多组学数据库
2021年9月30日,干细胞与再生医学研究院刘光慧研究组、曲静研究组和北京基因组研究所(国家生物信息中心)鲍一明研究组、张维绮研究组合作在 Nucleic Acids Research 杂志发表了题为“Regeneration Roadmap: database resources for regenerative biology”的论文,建立了再生生物学领域首个多组学数据库Regeneration Roadmap(RR)(https://ngdc.cncb.ac.cn/regeneration/index)。该数据库从转录组、单细胞转录组、表观基因组及药物基因组等不同层面整合了再生相关数据集,涉及11个物种、36种组织类型,实现了不同条件下基因表达随再生变化的汇聚融合,以及对不同层次组学数据的交互查询和联合比较分析。此外,数据库收录了基于已有文献报道的再生相关基因集,使得用户可以更加深入全面地了解特定基因或通路在再生生物学中的功能(图1)。
2021-09-30
随着细胞重编程、基因编辑、合成生物学、高通量测序等技术的快速发展,再生生物学进入前所未有的蓬勃发展时期,助力解决组织替代、功能修复、衰老干预、疾病治疗等一系列生命医学领域的重要科学难题。面对科学数据的爆炸式增长,亟需建立以再生生物学为核心的开放数据库,以存储世界范围内的组学研究数据为基础,推动再生相关的基础研究和临床转化应用的不断发展。
2021年9月30日,干细胞与再生医学研究院刘光慧研究组、曲静研究组和北京基因组研究所(国家生物信息中心)鲍一明研究组、张维绮研究组合作在 Nucleic Acids Research 杂志发表了题为“Regeneration Roadmap: database resources for regenerative biology”的论文,建立了再生生物学领域首个多组学数据库Regeneration Roadmap(RR)(https://ngdc.cncb.ac.cn/regeneration/index)。该数据库从转录组、单细胞转录组、表观基因组及药物基因组等不同层面整合了再生相关数据集,涉及11个物种、36种组织类型,实现了不同条件下基因表达随再生变化的汇聚融合,以及对不同层次组学数据的交互查询和联合比较分析。此外,数据库收录了基于已有文献报道的再生相关基因集,使得用户可以更加深入全面地了解特定基因或通路在再生生物学中的功能(图1)。
Regeneration Roadmap数据库首次实现了对多物种再生相关的不同层次组学数据的收录与整合。作为一个持续更新的国际化信息平台,Regeneration Roadmap 的建立为国内外再生生物学相关数据的统一汇交、集中存储、安全管理、开放共享以及前沿交叉研究和临床转化应用提供重要助力和支撑。该数据库对用户免费开放,相关运维团队将对该数据库进行定期维护与更新,不断整合更多的再生相关数据资源、汇交多层次组学数据。此外,该团队于2020年建立了Aging Atlas(AA)数据库(https://ngdc.cncb.ac.cn/aging/index),首次实现了对与衰老相关的不同层次多组学数据的收录和整合。目前Aging Atlas数据库已服务来自全球25个国家的上万名访问者。Aging Atlas和Regeneration Roadmap姊妹数据库将形成资源互补,共同推动衰老生物学和再生生物学的学科发展。
Regeneration Roadmap数据库由中国科学院动物研究所、中国科学院干细胞与再生医学科学数据中心、中国科学院干细胞与再生医学创新研究院、北京干细胞与再生医学研究院、中国科学院北京基因组所(国家生物信息中心)、首都医科大学宣武医院国家老年疾病临床研究中心等机构合作完成。中国科学院动物研究所刘光慧研究员、中国科学院北京基因组研究所(国家生物信息中心)鲍一明研究员、中国科学院动物研究所曲静研究员和中国科学院北京基因组研究所(国家生物信息中心)张维绮研究员为共同通讯作者。中国科学院北京基因组所(国家生物信息中心)硕士生康望、金彤和博士生张韬、中国科学院干细胞与再生医学创新研究院“致一”研究员马帅、首都医科大学博士生燕浩腾为共同第一作者。数据库的建设得到了中国科学院周琪院士、中国科学院干细胞与再生医学创新研究院胡宝洋研究员、中国科学院北京基因组研究所(国家生物信息中心)杨运桂研究员、首都医科大学宣武医院国家老年疾病临床研究中心王思研究员、中国科学院动物研究所宋默识研究员、中国科学院北京基因组研究所(国家生物信息中心)任捷研究员的指导和支持。该项目获得国家科技部、国家自然科学基金委、中国科学院和北京市等项目的资助。
文章链接:https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkab870/6378433
数据库(RR)链接:https://ngdc.cncb.ac.cn/regeneration/index
数据库(AA)链接:https://ngdc.cncb.ac.cn/aging/index
图1. Regeneration Roadmap数据库
